|
  Imprimer Imprimer
Une transformation
chimique n'est pas toujours totale et la réaction a lieu
dans les deux sens
I. Le pH
et sa mesure.
1. Définitions
d'un acide et d'une base selon Brönsted.
Un acide selon Brönsted
est une espèce chimique susceptible de céder un
ou plusieurs protons H+
Exemples :
le chlorure d'hydrogène
HCl
l'acide éthanoïque CH3COOH
l'acide méthanoïque HCOOH
Une base selon Brönsted
est une espèce chimique susceptible de capter un ou plusieurs
protons.
Exemples :
L'ion hydroxyde HO-
l'ion éthanoate CH3COO-
l'ammoniac NH3
2. Equation
de la réaction associée à une transformation
acido-basique.
2.1. Les deux couples mis en
jeu dans une transformation acido-basique.
Réaction de l'acide
propanoïque avec l'eau :
Il y a deux couples mis en
jeu :

2.2. Notation des deux couples
: acide / base
CH3CH2COOH / CH3CH2COO-
Acide propanoïque / ion propanoate
H3O+ / H2O
Ion oxonium / eau
3. Le pH
d'une solution aqueuses diluées.
On considère que les
solutions sont diluées quand leurs concentrations sont
 à 0,01
mol.L-1 à 0,01
mol.L-1
C'est le chimiste Danois Sorensen
qui proposa l'utilisation d'une échelle logarithmique
au lieu des concentrations des ions H3O+.
Définition du pH : pH
= -log [H3O+]
Si la concentration d'une solution
en ions oxonium [H3O+]= 4,8 x 10-5
mol.L-1
Le pH de la solution sera égal à -log [H3O+]
= -log (4,8 x 10-5) = 4,32

Question discussion réponse
:
Calculer le pH d'une solution
don't la concentration en ion [H3O+]= 2,5 x 10-3
mol.L-1
Comment varie le pH si la concentration [H3O+]augmente
?
Réponse :
pH = -log [H3O+]=
-log (2,5 x 10-3) = 2,6
quand [H3O+]augmente, le pH diminue.

Question discussion réponse
:
En vous aidant de votre calculatrice,
proposer un calcul permettant de determiner la concentration
en ions oxonium [H3O+] à partir d'une
valeur de pH.
Déterminer alors la
concentration [H3O+]d'une solution diluée
dont le pH est égal à pH = 3,52
Réponse :
[H3O+]= 10-pH
[H3O+] = 10-3,52
= 3,0 x 10-4 mol.L-1
II. La reaction
a lieu dans les deux sens.
Cette notion est mise en evidence
expérimentalement lors du TP.
1. Taux
d'avancement final d'une réaction non totale.
1.1. Symbolisme d'écriture
d'une réaction qui a lieu dans les deux sens.
CH3COOH(aq) + H2O = CH3COO-(aq)
+ H3O+(aq)
acide éthanoïque
eau ion éthanoate ion oxonium
1.2. Tableau de l'évolution
du système.
- La concentration en ion H3O+(aq)
est égale à [H3O+]= 10-pH
- V est le volume de la solution
- c est la concentration de CH3COOH introduit en solution
- xf est l'avancement final ; xf =
10-pH x V
- xmax est l'avancement maximal ; xmax=
cV

On a constaté pendant
le TP que xf < xmax
La réaction de l'acide
éthanoïque avec l'eau n'est donc pas totale.
1.3. Taux d'avancement final.
Dans l'expérience réalisée
en TP, on a déterminé que la réaction de
l'acide éthanoïque avec l'eau
A un taux d'avancement final de l'ordre de 4 %. t =
4 %
1.4. La réaction a lieu
dans les deux sens : il y a équilibre chimique.
En TP, on a montré que
les réactions ont lieu dans les deux sens :
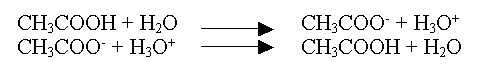
On dit alors que le système
est en équilibre et est noté :
CH3COOH + H2O =
CH3COO- + H3O+
non totale
équilibre
2. Les deux
réactions s'effectuent à la même vitesse.
On réalise à
nouveau une modélisation à l'état microscopique
selon les mêmes conditions que celles appliquées
dans le cours de chimie de cinétique (partie
A).
Mais on ajoute un cas particulier
(cas n°2) : celui où les produits réagissent
entre-eux pour redonner des réactifs.
20 BOULES ROUGES + 20 BOULES
BLEUES dans un récipient.
On tire au hasard 2 boules.
Cas n°1 : Si les boules
tirées sont rouge et bleue :
- tirer à pile ou face
avec une pièce de monnaie :
a. Si c'est pile (par ex.)
considère que le choc est efficace, alors retirer les
deux boules rouge et bleue et remplacer-les par une boule verte
et une boule jaune.
b. Si c'est face considère que le choc n'est pas efficace,
alors remettre les boules rouge et bleue dans le bécher.
Cas n°2 : Si les boules
tirées sont verte et jaune :
Considérer que le
choc est toujours efficace, alors retirer les deux boules verte
et jaune et remplace-les par une boule rouge et une boule bleue.
Cas n°3 : Si les boules
tirées ne sont pas rouge et bleue ou verte et jaune, remettre
les boules dans le becher.

Question discussion réponse
:
- Réaliser l'expérience
dans les conditions ci-dessus et noter vos résultats sous
la forme d'un graphe sur lequel vous représenterez l'évolution
du nombre de boules rouges et de boules vertes. Effectuer environ
200 tirages.
- Est-ce qu'au bout d'un temps suffisamment long la valeur xmax
= 20 est atteinte ?
- Quelle est la valeur atteinte ? On notera xf cette valeur.
- En déduire le taux d'avancement final de cette réaction
?
- Les deux réactions inverses se déroulent-elles
à la même vitesse ?
Réponse :
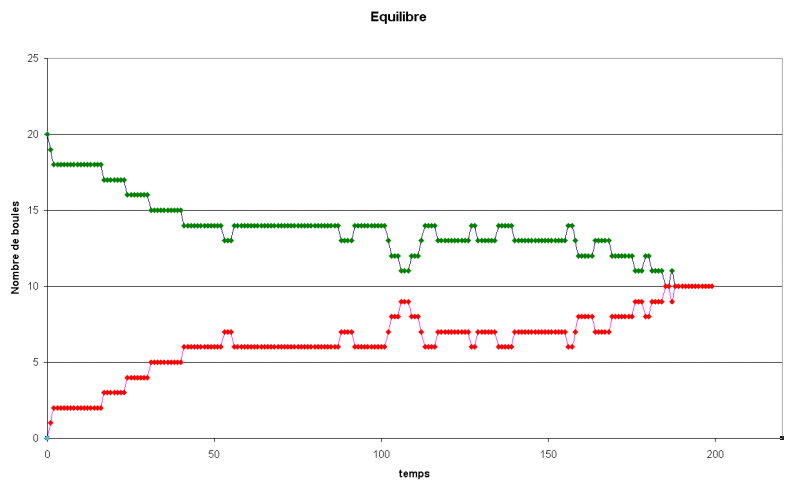
- La valeur maximale de l'avancement
n'est pas atteinte.
- La valeur atteinte à l'équilibre est xf =
10
-
- Les deux réactions se déroulent à la même
vitesse. Elles atteignent l'équilibre en même temps.
Conclusion :
- Les réactions inverses
ont lieu à la même vitesse.
- Les molécules de réactifs et de produits n'ont
pas la même probabilité de chocs efficaces.
  Imprimer Imprimer
Etat d'équilibre
d'un système
I. Quotient de réaction
Qr.
1. Définition
du quotient de réaction.
Le quotient de réaction
permet de préciser l'état du système en
évolution.
- On ne tient compte dans le
quotient de réaction que des espèces dissoutes.
(c-à-d. pas les solides).
- On ne tient pas compte du solvant (eau).
- Les espèces dissoutes
sont caractérisées par leur concentration molaire
volumique 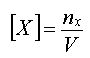 (mol.L-1)
(mol.L-1)
Pour une réaction aA(aq)
+ bB(aq) = cC(aq) + dD(aq), le quotient de réaction associé
à cette réaction s'écrit :

Le quotient de réaction
est lié à une équation de réaction
dans un sens donné.
2. Détermination
de l'expression de Qr en solution aqueuse homogène.

Question discussion réponse
:
Compléter les lignes
vides de chaque tableau.



Réponse :
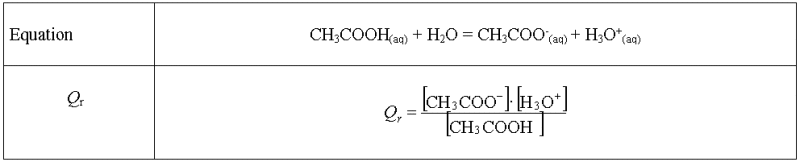
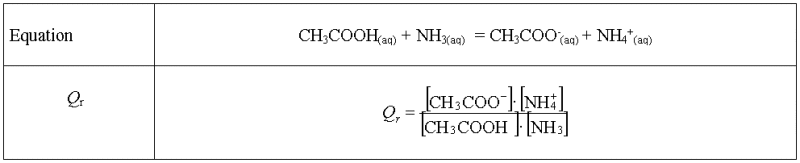
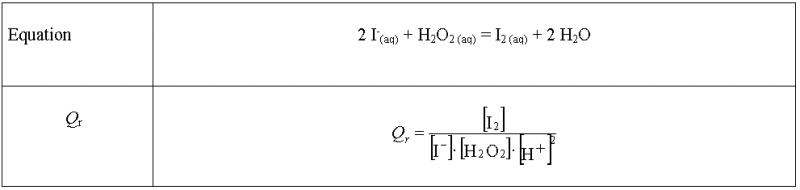
On ne fait apparaître
l'eau car dans ces cas, l'eau est le solvant.

Attention : vous verrez plus
tard dans l'année les réactions d'estérification
dans lesquelles l'eau n'est pas le solvant mais un produit de
la réaction.
Dans ce cas l'eau, rentre dans l'expression du quotient de réaction.
3. Détermination
de l'expression de Qr en solution aqueuse hétérogène.

Question discussion réponse
:
Ecrire l'expression de Qr dans
chaque cas :



Réponses :
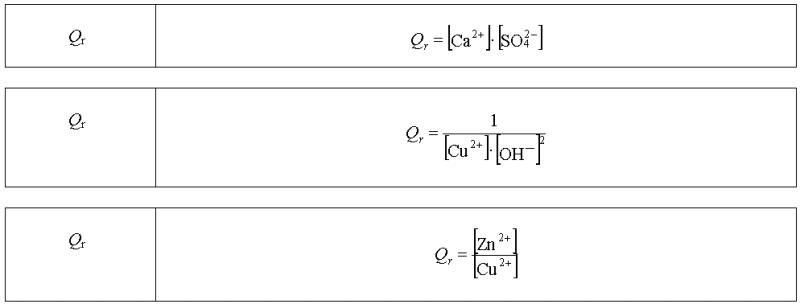
On ne fait pas apparaître
les espèces chimiques solides, on leur affecte la valeur
1.
II. Quotient de réaction dans l'état d'équilibre
Qr, eq.
1. Définition
de Qr,
eq.
Qr, eq =
Qr quand l'état d'équilibre du système
chimique est atteint.
Dans cet état les concentration
[X]eq ne varient plus.
Par la suite, il sera intéressant
de comparer Qr,
eq et Qr
2. Détermination
de la valeur de Qr, eq par conductimétrie.
Cette partie est abordée
en TP
2.1. Rappels de conductimétrie.
Page 122 figure 5, 6 et 7
Schéma du dispositif
:

- Le générateur
noté G fournit une tension alternative (pour éviter
les phénomènes d'électrolyse aux bornes)
de fréquence f = 1000 Hz.
- Une mesure de U et de I est réalisée.
- La valeur de la résistance de la solution est ainsi
déterminée. U = RI.
- Le conductimètre donne la valeur de la conductance G
= 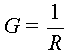 G
s'exprime en Siemens (S) G
s'exprime en Siemens (S)
- G dépend des caractéristiques de la cellule
(l et S). On note k la constante de cellule.
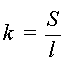
G = ks
La conductivité s dépend :
o des concentrations des ions en solution.
o d'une grandeur caractéristique de chaque ion, la conductivité
molaire volumique l.
Exemple : pour une solution
de nitrate d'argent en solution aqueuse (en négligeant
H3O+et HO-)
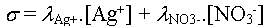
L'objectif d'une mesure conductimétrique
est de :
- déterminer une concentration
ionique. Mesure de G , puis on en déduit s, puis [X-].
- déterminer l'équivalence lors d'un titrage.
2.2. Détermination expérimentale de Qr, eq.
Cette partie est vue en TP.
2.2.1. Principe.
- On introduit dans un ballon
un volume V d'une solution acide de concentration c.
- On place dans la solution, la cellule du conductimètre
préalablement calibré avec une solution étalon.
- On lit la valeur de la conductivité s.
2.2.2. Détermination
de Qr, eq.
Soit l'équation de la
réaction : 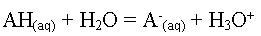
Données : c,
l (H3O+) et l (A-)
Mesure : s ou G Remarque : si on mesure
G alors 
- On écrit l'expression
de la conductivité 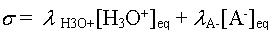
- La réaction étant équimolaire, on a [H3O+]
= [A-]
- On déduit que 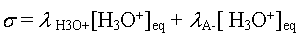 et
et 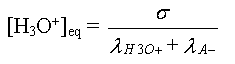
- On écrit la conservation de la matière :
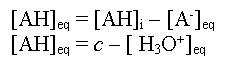
- On en déduit l'expression
de Qr, eq en fonction de [H3O+]

- A partir de la valeur de
s trouvée expérimentalement, on
trouve la valeur de
avec l'expression 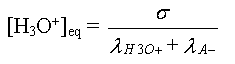
- On en déduit la valeur de Qr, eq.
III. Constante d'équilibre K associée à
l'équation d'une réaction, à une température
donnée.
1. Qr, eq
dépend-il de la composition initiale du système
?

Question discussion réponse
:
Soit la réaction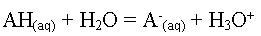
- on connaît la concentration
c de l'acide AH.
- on mesure s pour différentes valeurs de
c.
- on en déduit par la méthode vue précédemment
les valeurs de Qr,
eq.
Avec 
Compléter le tableau
suivant :
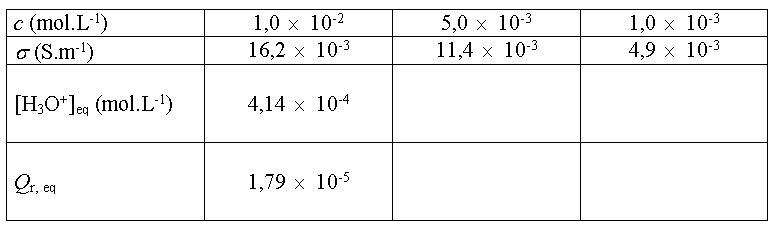
Conclusion : La valeur de Qr, eq
est ……………………de la composition
initiale du système.
Réponse :

Conclusion : La valeur de Qr, eq
est indépendante de la composition initiale du système.
2. Définition
de la constante d'équilibre K.
La constante d'équilibre
associée à l'équation d'une réaction
est la valeur que prend le quotient de réaction dans l'état
d'équilibre du système.
K = Qr, eq
- K dépend de
la réaction
- K dépend de la température
- K ne dépend pas de la composition initiale du
système.
IV. Influence de l'état initial d'un système
et de la constante d'équilibre K sur le taux d'avancement
final d'une réaction.
1. Influence
de la composition initiale sur t.
Soit 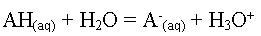

Question discussion réponse
:
Compléter le tableau
suivant :
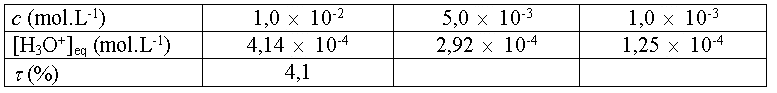
Conclusion : t
…………… de c
Réponse :
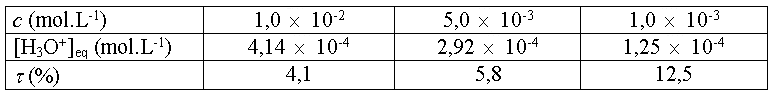
Conclusion :t
dépend de c.
Plus la solution d'acide est
diluée, plus le taux d'avancement final de la réaction
de l'acide avec l'eau est élevé.
Quand c diminue, t
augmente.
2. Influence
de la constante d'équilibre K.
Soit 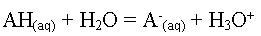

Question discussion réponse
:
Analyser le tableau suivant
:

Conclusion : t
…………… de K
Réponse :
Conclusion : t
dépend de K.
Plus la constante d'équilibre
est élevée, plus le taux d'avancement final de
la réaction de l'acide avec l'eau est élevé.
Quand t augmente,
t augmente.
  Imprimer Imprimer
Transformations
associées à des réactions acido-basiques
en solution aqueuse
I. Autoprotolyse de l'eau.
1. pH de
l'eau pure.
A 25°C pH = 7 alors [H3O+]
= 10-pH= 1,0 x 10-7 mol.L-1
2. Autoprotolyse de l'eau.
H2O + H2O = H3O+(aq) + HO-(aq)
[H3O+] = [HO-] =
1,0 x 10-7 mol.L-1

Question discussion réponse
:
La réaction d'autoprotolyse
de l'eau est-elle avancée ?
Pour répondre à
cette question vous :
- calculerez xf
- calculerez la quantité (en mol) d'eau contenue dans
1 L.
- Etablirez un tableau d'évolution du système
- Calculerez xmax
- En déduirez la valeur de
t
Conclusion : la réaction
d'autoprotolyse de l'eau est ………………………….
On prendra un volume V
= 1 L d'eau pure.
Données : Masse molaire
de l'eau M = 18 g.mol-1
Masse volumique de l'eau m
= 1 g.cm-3
Réponse :
Dans un premier temps, déterminons
xf
xf = 10-pH
x V = 1,0 x 10-7 x 1 = 1,0 x 10-7
mol
Dans un second temps déterminons
la quantité de matière d'eau (mol) contenue dans
un litre.
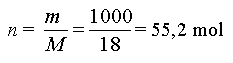
Dans un troisième temps,
on établit le tableau d'évolution :
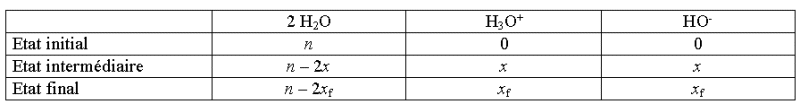
Dans un quatrième temps, on calcule xmax
Si la réaction était
totale, on aurait : n - 2xmax = 0
55,2 - 2xmax
= 0 xmax = 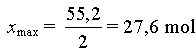
Dans un cinquième temps,
on détermine le taux d'avancement final 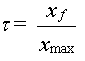
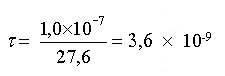
Conclusion : la réaction
d'autoprotolyse de l'eau est très peu avancée.
3. Produit
ionique de l'eau Ke.
La réaction 2 H2O
= H3O+(aq) + HO-(aq) est un
équilibre.
On peut donc écrire
que Ke = [H3O+] [HO-] = 1,0
x 10-7 x 1,0 x 10-7 = 1,0 x 10-14
à 25°C.
Autre notation :
pKe = -log
Ke
pKe = 14 à 25°C
On notera que Ke
dépend de la température. (voir page 138, figure
4)
Quand la température augmente, Ke augmente alors le pKe
diminue.
En effet, une élévation
de température favorise la dissociation des molécules
d'eau. La quantité d'ions H3O+ et HO- est
ainsi plus importante, donc Ke augmente.
4. Echelle
de pH.

II. Constante d'acidité
KA et pKA.
1. Définition.
La constante d'acidité
KA est la constante d'équilibre associée à
l'équation de la réaction d'un acide avec l'eau.
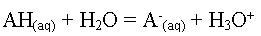
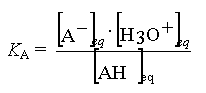
On note pKA = - log
KA ou encore KA = 10-pKA
Exemple :
A 25 °C la constante d'acidité
du couple acide benzoïque / ion benzoate est KA
= 6,5 x 10-7
Alors pKA = 4,2
2. Cas particuliers
des couples de l'eau.


3. Comparaison
du comportement en solution à concentration identique,
des acides entre-eux et des bases entre-elles.
3.1. Cas des acides.
Cette partie est étudiée
lors des TP.

Question discussion réponse
:
- A partir des données
fournies dans le tableau suivant, formuler une hypothèse
quant au comportement des acides étudiés en solution.
Quel est l'acide qui se dissocie le plus dans l'eau ?
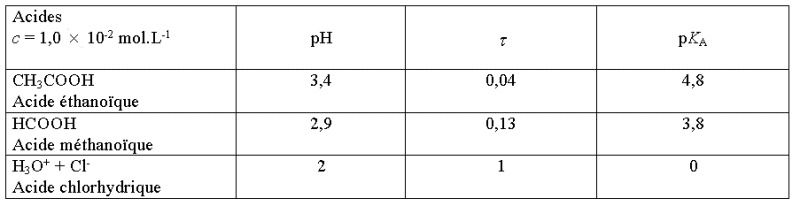
Réponse :
Un acide A1 se dissocie plus
qu'un acide A2, si à concentration égale, le taux
d'avancement final de sa réaction avec l'eau est plus
grande. t1
> t2.
Acidité croissante :
CH3COOH (Acide éthanoïque)
< HCOOH (Acide méthanoïque) < H3O+
+ Cl- (Acide chlorhydrique)
L'acide chlorhydrique est l'acide
qui se dissocie le plus dans l'eau.
3.2. Cas des bases.

Question discussion réponse
:
- A partir des données
fournies dans le tableau suivant, formuler une hypothèse
quant au comportement des bases étudiées en solution.
Quel est la base qui réagit le plus avec l'eau ?
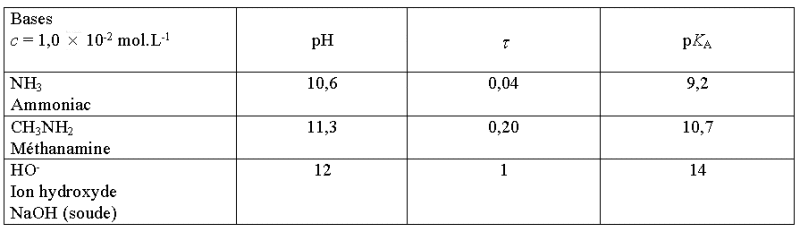
Réponse :
Une base B1 réagit plus
avec l'eau qu'une base B2, si à concentration égales,
le taux d'avancement final de sa réaction avec l'eau est
plus grand. t1
> t2.
Basicité croissante
:
NH3 (Ammoniac) < CH3NH2
(Méthanamine) < HO- (Ion hydroxyde)
La soude est la base qui réagit
le plus avec l'eau.
III. Détermination de la constante d'équilibre
associée à une réaction acido-basique.
1. Autoprotolyse
de l'eau.
2 H2O = H3O+(aq) +
HO- (aq)
Ke = [H3O+]
x [HO-]
K = [H3O+] x [HO-]
K = Ke
2. Réaction
d'un acide avec l'eau.
AH(aq)
+ H2O = A-(aq)
+ H3O+
K = 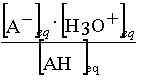
KA = 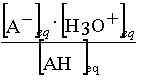
K = KA
3. Réaction
d'une base avec l'eau.
A-(aq) +
H2O = AH(aq) + HO-(aq)
K = 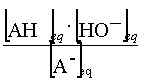
Reprenons l'expression de la
constante d'acidité associée à la réaction
AH(aq) + H2O = A-(aq) +
H3O+
KA = 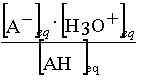

Astuce : Multiplier par [H3O+]eq
le numérateur et le dénominateur de l'expression
de K
K =  
On retrouve l'expression de
Ke = [H3O+] x [HO-]au numérateur
et 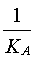

4. Réaction
d'un acide avec une base.
Soit la réaction suivante
:
CH3COOH(aq) + NH3 (aq)
= CH3COO-(aq)
+ NH4+(aq)
Dans un premier temps on écrit
:
Couple 1 : CH3COOH /
CH3COO-
Equation associée à
la reaction CH3COOH avec l'eau : CH3COOH(aq)
+ H2O = CH3COO-(aq) + H3O+(aq)
Constante d'acidité
associée : KA1 = 
Dans un deuxième temps,
on écrit :
Couple 2 : NH4+
/ NH3
Equation associée à
la reaction NH4+ avec l'eau : NH4+(aq) +
H2O = NH3 (aq) + H3O+(aq)
Constante d'acidité
associée : KA2 = 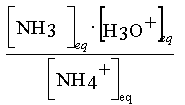
Dans un troisième temps,
on écrit la constante d'équilibre associée
à la réaction :
CH3COOH(aq) + NH3 (aq)
= CH3COO-(aq) + NH4+(aq)
K = 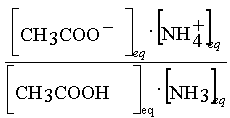

Astuce : Multiplier par [H3O+]eq
le numérateur et le dénominateur de l'expression
de K
K = 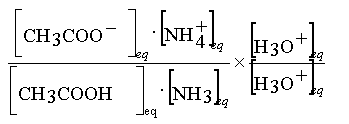
On retrouve l'expression de KA1 et de 
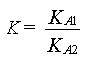
IV. Diagrammes de prédominance et de distribution d'espèces
chimiques acide et basiques en solution.
1. Définition
de la prédominance.
Une espèce est prédominante
devant une autre si sa concentration dans la solution est supérieure
à celle de cette autre espèce.
2. Relation
entre pH et pKA permettant de définir
un domaine de prédominance.
On étudie une espèce
chimique acido-basique pouvant exister sous la forme acide AH
et la forme basique A-.

3. Domaine
de prédominance d'un indicateur coloré.
Voir le TP
correspondant.
Exemple : le rouge de chlorophénol
Le rouge de chlorophénol
est un indicateur utilisé lors des titrages acido-basiques.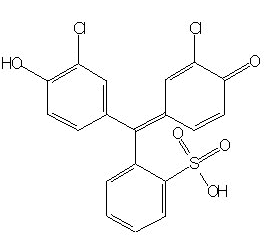
Sa formule chimique (hors programme) est :
Il existe sous deux formes.
- une forme acide notée
HInd de couleur jaune
- une forme basique notée Ind- de couleur rouge
Le pKA de ce couple Hind /
Ind- est égale à pKA = 5,6
Les domaines de prédominance
sont délimités par rapport au pKa du couple Hind
/ Ind- .
On considère que si
l'indicateur coloré se trouve dans une solution dont le
pH < pKA -1
c'est à dire pH < 4,6 , il prend une couleur jaune.
Expérimentalement, il prend la couleur jaune à
partir d'une valeur de pH < 4,8.
De même, on considère
que s'il se trouve dans une solution dont le pH > pKA
+ 1 c'est à dire 6,6, il prend une couleur rouge.
Expérimentalement, il prend la couleur rouge à
partir de pH > 6,4.
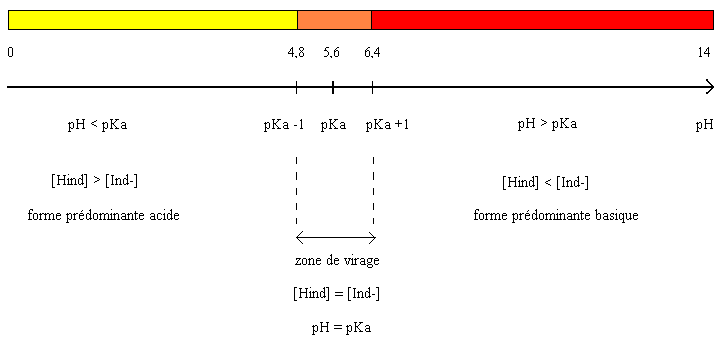
4. Distribution
des espèces acido-basiques du rouge de chlorophénol.

En TP,
la distribution des espèces acido-basiques du bleu de
bromothymol sera établi.
V. Titrage
pH-métrique.
1. Objectif et conditions d'un titrage pH-métrique.
Objectif : titrer une solution c'est déterminer la concentration
molaire de cette solution.
Conditions : pour qu'une réaction
puisse être une réaction de titrage, il faut que
:
- La transformation soit quasi-totale
K > 104
- La transformation soit rapide.
2. Matériels.
- pH mètre et son électrode.
- Burette graduée contenant l'espèce titrante
- Becher contenant l'espèce à titrer
- Agitateur magnétique et son turbulent (barreau aimanté)
3. Protocole.
- On verse à l'aide
d'une pipette jaugée un volume déterminé
de la solution à titrer dans le bécher.
C'est ce volume qu'on utilisera dans les calculs.
Attention, les pipettes peuvent être à un trait
ou deux traits.
- On ajoute de l'eau distillée si nécessaire afin
que l'électrode trempe bien dans la solution.
Cet ajout ne change pas le volume à l'équivalence.
Seule l'allure de la courbe pH-métrique change.
- On étalonne le pH-mètre à l'aide d'une
solution tampon de pH connu.
Selon les pH-mètres, il faut une ou deux solutions tampons
de pH différents.
- On essuie délicatement l'électrode et on la trempe
dans la solution à titrer.
- On verse à l'aide de la burette la solution titrante
mL par mL.
Attention, à l'approche du saut de pH, diminuer la quantité
versée de solution titrante.
- On mesure le pH pour chaque volume ajouté.
4. Définition
de l'équivalence.
A l'équivalence, les
quantités de l'espèce à titrer introduite
initialement dans le bécher et de l'espèce titrante
sont égales dans les proportions stoechiométriques.
ni (espèce titrée)
= n (espèce titrante versée)
5. Quelques
exemples de titrages.
Courbes obtenues sur le site
: http://www2.cegep-st-laurent.qc.ca/depar/chimie/solution/cour.htm
Dans chaque cas, deux courbes
sont représentées :
- les valeurs du pH pour chaque
volume de solution titrante versée. (en rouge).
- La dérivée (en bleu) .
Cette courbe est pratique pour déterminer avec précision
de volume à l'équivalence
- Le volume de solution à
titrer est égale à 10,0 mL.
- La concentration de la solution titrante est c = 0,020 mol.L-1

Question discussion réponse
:
Dans chaque cas :
- déterminer le volume
et le pH à l'équivalence.
- En déduire la concentration c0 de la
solution titrée.
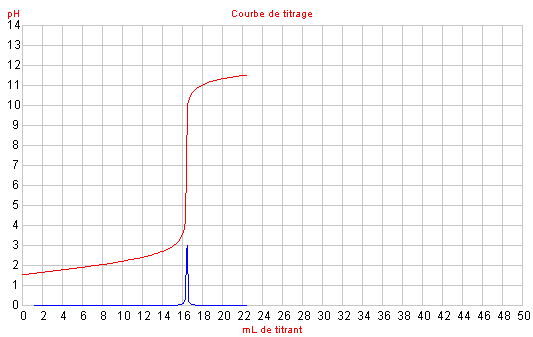
Cas n° 1 : Titrage de l'acide
chlorhydrique (dissociation totale dans l'eau) par la soude (dissociation
totale dans l'eau).
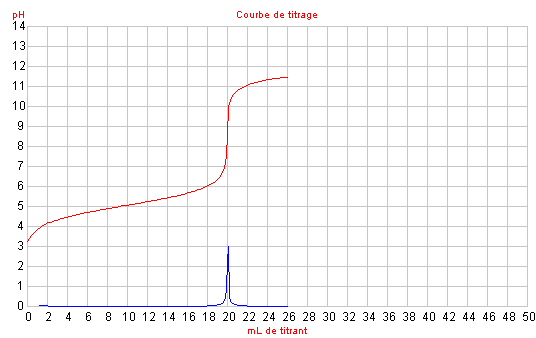
Cas n° 2 : Titrage d'un acide (dissociation partielle dans
l'eau) par la soude (dissociation totale dans l'eau).
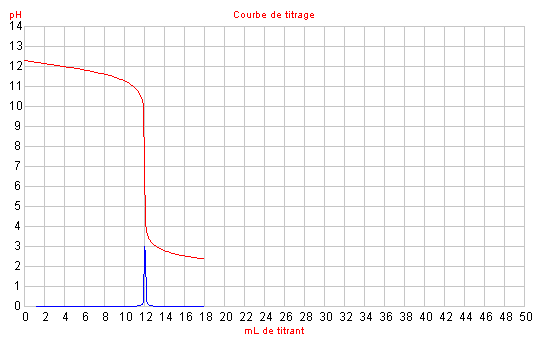
Cas n° 3 : Titrage de la
soude (dissociation totale dans l'eau) par l'acide chlorhydrique
(dissociation totale dans l'eau).
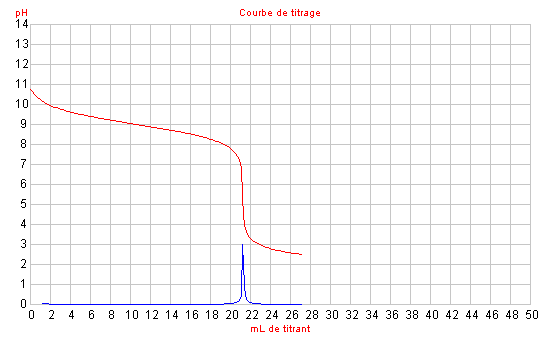
Cas n° 4 : Titrage d'une
base (dissociation partielle dans l'eau) par l'acide chlorhydrique
(dissociation totale dans l'eau).
Réponses :
Cas n° 1 : VE = 16,5 mL
pHE = 7
Cas n° 2 : VE = 20,0 mL
pHE = 8,4
Cas n° 3 : VE = 12,1 mL
pHE = 7
Cas n° 4 : VE = 21,0 mL
pHE = 6,0
A l'équivalence, on
a : 
Cas n° 1 : c0 =
3,30 x 10-2 mol.L-1
Cas n° 2 : c0 =
4,00 x 10-2 mol.L-1
Cas n° 3 : c0 =
2,42 x 10-2 mol.L-1
Cas n° 4 : c0 =
4,20 x 10-2 mol.L-1
6. Choix
de l'indicateur coloré dans le cas d'un titrage colorimétrique.
On choisit l'indicateur coloré
de telle manière à ce que la zone de virage de
l'indicateur encadre la valeur du pHE.
(On notera que si le saut de
pH est dans le domaine de la zone de virage, l'indicateur conviendra).

Question discussion réponse
:
En vous aidant du tableau de
données de quelques indicateurs colorés ci-dessous,
proposer le ou les indicateurs colorés pouvant être
utilisés pour les quatre titrages vus précédemment.

Réponse :
Cas n° 1 : Bleu de bromothymol
6,0 < pHE = 7,0 < 7,6
Rouge de phénol 6,8 < pHE = 7,0 < 7,6
Cas n° 2 : Phénolphtaléine
8,2 < pHE = 8,4 < 10,0
Rouge de crésol 6,8 < pHE = 8,4 < 8,4
Cas n° 3 : Bleu de bromothymol
6,0 < pHE = 7,0 < 7,6
Rouge de phénol 6,8 < pHE = 7,0 < 7,6
Cas n° 4 : Rouge de méthyle
4,8 < pHE = 6,0 < 6,0
Bleu de bromothymol 6,0 < pHE = 6,0 < 7,6
7. Qu'en
est-il des transformations totales ?
L'une des conditions pour qu'une
réaction soit utilisable en tant que réaction de
titrage est qu'elle doit être quasi-totale.
Est-ce cas pour les réactions
de titrages que nous avons étudiés ?
Cas n°1 : H3O+
+ HO-1(aq) = 2 H2O
A l'équivalence :
- pHE = 7,0
- Le volume totale de la solution est Vtotal =
10,0 + 21,0 = 31,1 mL
- La quantité de base HO- introduite est n
HO- = cV = 0,020 x 21,1 x 10-3=
4,22 x 10-4 mol
- La quantité d'ions HO- restant dans le milieu
est :
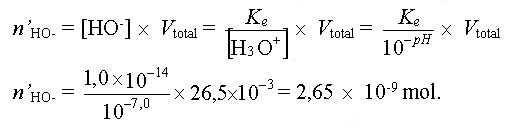
- Le taux d'avancement final est donc égale à 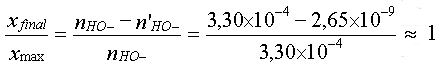
- La réaction de titrage est donc quasi totale.

Question discussion réponse
:
Montrer que la réaction
de titrage du cas n° 4 est également quasi-totale.
Réponse :
A-(aq) +
H3O+ = AH(aq) + H2O
A l'équivalence :
- pHE = 6,0
- Le volume totale de la solution est Vtotal =
10,0 + 21,0 = 31,0 mL
- La quantité d'acide H3O+ introduite est n H3O+ = cV = 0,020 x 21,0 x 10-3 = 4,22
x 10-4 mol
- La quantité d'ions H3O+ restant dans le milieu
est :
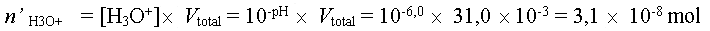
- Le taux d'avancement final est donc égale à 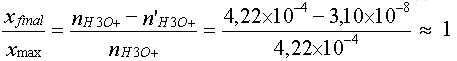
- La réaction de titrage est donc quasi totale.
Les mêmes calculs pour
les cas n°2 et n°3 aboutiront au même résultat.
Conclusion : les réactions
de titrages faisant intervenir les ions H3O+
et/ou HO- sont quasi-totales.
|