|
  Imprimer Imprimer
Fiche de révision
bac
Une transformation
chimique n'est pas toujours totale et la réaction a lieu
dans les deux sens
Mots-clés, connaissances
à savoir
Acide selon Brönsted
Base selon Brönsted
Couple acide / base
pH = - log [H3O+]
[H3O+] = 10-pH
Avancement final xf
= 10-pH x V
Taux d'avancement final 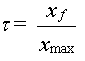
|
Savoir faire à maîtriser
Savoir écrire
l'équation de la réaction associée à
une transformation acido-basique
Savoir identifier les deux couples mis en jeu dans cette équation
Savoir calculer l'avancement final de la réaction à
partir du pH
|
  Imprimer Imprimer
Fiche de révision
bac
Etat d'équilibre
d'un système
Mots-clés, connaissances
à savoir
Quotient de réaction

Qr, eq quotient de réaction à
l'équilibre
Seules les espèces dissoutes interviennent dans l'expression
de Qr
Le solvant n'intervient pas dans l'expression de Qr
Les espèces solides n'interviennent pas dans l'expression
de Qr
Constante d'équilibre K = Qr, eq
L'équilibre est dynamique
Les quantités de matière n'évoluent plus
à l'équilibre
Qr, eq est indépendant des conditions initiales (concentrations)
Le taux d'avancement final t dépend de la constante d'équilibre
K
Le taux d'avancement final t
dépend de l'état
initial du système (concentrations)
|
Savoir faire à maîtriser
Savoir utiliser la
relation 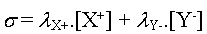 avec éventuellement G = ks avec éventuellement G = ks
Savoir donner l'expression littérale de Qr
à partir de l' équation d'une réaction
|
  Imprimer Imprimer
Fiche de révision
bac
Etat d'équilibre
d'un système
Mots-clés, connaissances
à savoir
Produit ionique
de l'eau Ke = [H3O+] x [HO-]
Acide pH < 7 ; basique pH > 7
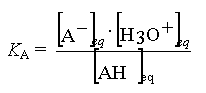
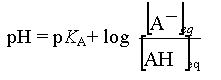 Zone de virage d'un
indicateur coloré
Zone de virage d'un
indicateur coloré
Domaine de prédominance (échelle de pH)
Distribution des espèces acides et basiques (courbes %
en fonction du pH)
Les réactions de titrage sont quasi-totales
|
Savoir faire à maîtriser
Savoir déterminer
le pH à partir des concentrations [H3O+]
et [HO-] avec Ke = [H3O+] x [HO-] et
pH = -log [H3O+]
Savoir déterminer une constante d'équilibre K,
à partir de KA et Ke
Savoir identifier une espèces prédominante en connaissant
le pH et le pKA
Savoir réaliser un titrage pH-métrique
Savoir déterminer un volume à l'équivalence
Savoir choisir convenablement un indicateur coloré pour
un titrage
|
|