|
  Imprimer Imprimer
Interrogation
Date : lundi 8 novembre 2004 Durée : 10 min
Couleur de la solution
de dichromate de potassium.
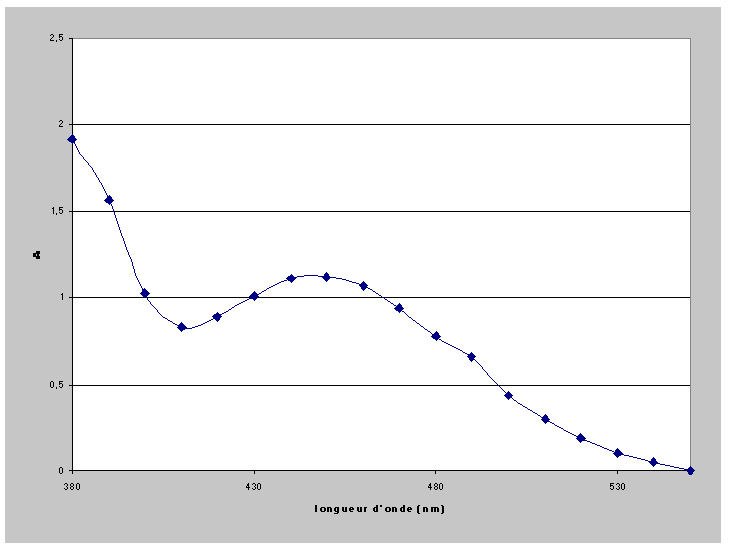
Le graphe ci-dessous donne
l'absorbance A d'une solution de dichromate de potassium,
de concentration molaire
c = 4,0 x 10-3 mol.L-1 pour différentes
longueurs d'onde.
La longueur de la cuve est l = 1,0 cm.
1. Donner la couleur de la
solution de dichromate de potassium. Justifier rigoureusement
votre réponse.
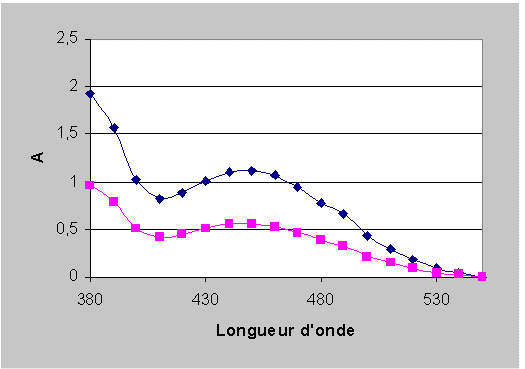
2. Sur le graphique ci-contre, représenter A =
f (l) pour une solution de dichromate de
potassium
de concentration c' = 2,0 x 10-3 mol.L-1
. Justifier rigoureusement votre réponse.
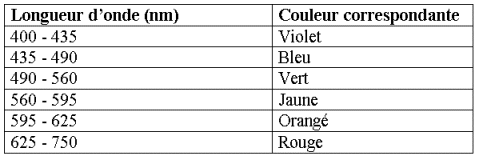
Données :
  Imprimer Imprimer
Correction: La couleur du dichromate de potassium.
1. La couleur de la solution
est orange car les longueurs d'onde non absorbées ont
une valeur supérieures
à 560 nm.Ainsi, le jaune, l'orange et le rouge ne sont
pas absorbés. Rouge + Jaune = Orange.
2.
2. La loi de Beer-Lambert s'écrit A = kc avec
k = e l
Si la concentration est 2 fois plus faible alors l'absorbance
est divisée par 2.
  Imprimer Imprimer
Extrait de l'examen
blanc ''Les Borgs"
EPISODE III : L'ASSIMILATION
DU VOYAGEUR TEMPOREL MORIN
Pendant que les membres de
l'USS enterprise essayent de comprendre le mécanisme
des borgs, Jean Luc Picard reçoit un message d'un voyageur
temporel. Celui provient de
Philippe Morin, qui sous son activité de professeur de
Sciences Physiques en l'année 2005,
n'est autre que l'un des représentants de la guilde temporelle
chargée de la stabilité du flux temporel.
Lors d'une mission en 2366,
il fut capturer par les Borgs qui ont commencé
son assimilation. Cette assimilation consiste à le transformer
en Borg à la suite d'une injection
d'un produit chimique : le Borg-H. Il réussi à
s'échapper grâce à son transphaseur temporel
et trouver refuge sur l'USS Enterprise. Il demande maintenant
au capitaine Picard de lui venir
en aide pour annuler son assimilation.

Vous observerez sur la photo qu'un tuyau relie la combinaison
Borg au cerveau de Philippe
Morin. Il sert au transfert du Borg-H qui le transforme en Borg.
Le voyageur Morin en phase d'assimilation, mais optimiste sur
les solutions que DATA va trouver.
DATA comprend très vite
qu'il faut réussir à lui injecter un antidote.
Mais il faut deux conditions pour que l'antidote soit efficace
:
- Il faut connaître exactement la vitesse volumique instantanée
d'action du Borg-H.
- Il faut injecter l'antidote exactement à la date correspondant
au temps de demi-réaction.
DATA reproduit la réaction
dans son laboratoire en mettant en contact 500 mg de Borg-H solide
et une solution d'antidote A. Cette réaction entraîne
la formation d'un gaz G selon l'équation : Borg-H + A
= G
1. On introduit 10 mL de la
solution d'antidote A de concentration 0,5 mol.L-1
dans un ballon. Vérifier que la solution d'antidote permet
la consommation totale de Borg-H
(la masse molaire de Borg-H est M = 180 g.mol-1)
La réaction est suivie par mesure de la pression à
l'intérieure d'une enceinte très étanche,
car le Borg-H peut contaminer le vaisseau.
Schéma de principe avant
la mise en contact des réactifs

- L'apparition du gaz, en supplément
de l'air déjà présent, crée une surpression
p mesurée au pressiomètre.
- Lorsque le ballon est placé verticalement, le Borg-H
tombe dans la solution et la réaction "démarre
".

2. Le suivi expérimental
de la pression donne la courbe 1 ci-dessous.

Montrer que si p est exprimé
en Pascal et n en mol, on a sensiblement n = 1,21 x 10-7
p.
La courbe 2 donne l'évolution
de la quantité de matière en gaz en fonction du
temps.

3. Définir et déterminer
graphiquement la vitesse volumique instantanée (en mol.L-1.s-1)
de formation du gaz à la date t0.
4. Peut-on estimer à partir de la courbe que la réaction
est terminée ? Justifier votre réponse.
5. Déterminer le temps de demi-réaction de cette
réaction. Justifier.
6. Déterminer la quantité de matière gazeuse
formée au cours de la réaction.
7. Etablir la relation entre la quantité de gaz formée
n et la quantité de Borg-H consommé nBorg-H.
8. En déduire la masse de Borg-H consommé au bout
de 600 s. A-t-il été complètement consommé
?
DATA a mis beaucoup trop de
temps pour réaliser son expérience, mais Philippe
Morin a quand même été sauvé car DATA
a fait un saut temporel vers le passé proche pour injecter
l'antidote au bon moment.
  Imprimer Imprimer
Correction
Episode III
1. nborg-H
= m / M = 2,8 x 10-3 mol. D'autre part on dispose
de 10 mL d'antidote A de concentration 0,5 mol.L-1
alors
n = C V = 0,5 0,010 = 5,0 x 10-3 mol 0,5 point
La quantité d'antidote est bien supérieure à
la quantité de Borg-H.
2. On a pV = nRT alors  = 1,27
x 10-7p 0,5 point = 1,27
x 10-7p 0,5 point
3. La vitesse volumique instantanée de formation du gaz
est v =  0,5
point 0,5
point
On détermine graphiquement le coefficient de la tangente
à la courbe à la date t0.
On trouve  = 2,5 x 10-5 0,5 point
= 2,5 x 10-5 0,5 point
Alors v = 2,5 x 10-5 / 0,300 = 8,33 x 10-5
mol.L-1.s-1 0,5 point
4. On constate que la vitesse est pratiquement nulle au-delà
de 500 s, on peut alors considérer que la réaction
est terminée. 0,5 point
5. Le temps de demi-réaction
est la date à laquelle on a xmax / 2 ; par lecture graphique,
on trouve 0,0025 / 2 = 0,00125 mol
qui correspond à la date t1/2 = 60 s. 0,5 point
6. on trouve par lecture graphique
n = 0,0025 mol. 0,5 point
7. La réaction étant
équimolaire, on a n = nBorg-H
= 0,0025 mol. 0,5 point
8. mBorg-H =
nM = 0,0025 x 180 = 0,450 g ; Le Borg-H n'a pas été
complètement consommé. 0,5 point |