|
  Imprimer Imprimer
TP n° 4 : Mise
en évidence expérimentale de réactions lentes
et de différents facteurs cinétiques
Objectif : Mettre en évidence
des réactions lentes et différents facteurs cinétiques
I. Influence
des concentrations molaires
Réactions entre les
ions thiosulfate et l'acide chlorhydrique
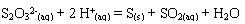
On étudie la cinétique
de production de soufre qui entraînera la coloration du
milieu.
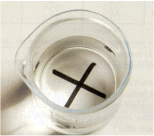
On note le temps t auquel la croix disparaîtra.
· Sur 6 bouts de papier,
dessiner 6 croix et poser 6 béchers dessus.
Expérience
A :
· Effectuer les mélanges
suivants : 4 gouttes de HCl à 6,0 mol.L-1 (Attention
DANGER).
dans 30,0 mL de thiosulfate de concentration Ci
· Compléter le tableau

Expérience
B :
· les mélanges suivants : 2,0 mL de HCl de concentration
Ci
dans 10,0 mL de thiosulfate de concentration 10-1
mol.L-1
· Compléter le tableau

Questions et interprétation
:
1. Quel est l'objectif de l'expérience
A ?
2. Quel est l'objectif de l'expérience B ?
3. Que montre l'expérience A ?
4. Que montre l'expérience B ?
Conclusion : Une transformation
chimique est d'autant plus ………………..
que la concentration des ………………..
II. Influence de la température.
A. Dissolution
d'un comprimé d' Alka-Seltzer.
L' Alka-Seltzer contient un
mélange de dihydrogénophosphate de calcium, d'hydrogénocarbonate
de sodium, de l'acide citrique et de l'aspirine (acide acétylsalicylique).
Dans l'eau, s'effectuent les réactions suivantes :
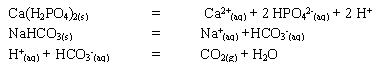
o Remplir deux béchers
de 250 mL avec environ 200 mL d'eau: l'un d'eau froide (avec
quelques glaçons), l'autre d'eau chaude.
o Jeter en même temps deux comprimés d'Alka-Seltzer.
Questions et interprétation
:
1. Quelle est l'influence de
la température sur la dissolution des comprimés
d'Alka-Seltzer.
2. Quel est le nom du gaz qui se dégage ? Par quel test
pourrait-on l'identifier ?
3. Avec quel(s) instrument(s) pourrait-t-on effectuer une mesure
quantitative de son dégagement ?
Conclusion : Une transformation
chimique est ……………………………
lorsque la température est ………………
B. Test
de présence du glucose (fonction aldéhyde) avec
la liqueur de Fehling.
Expérience réalisée par le professeur devant
la classe.
o Dans deux tubes à
essais, on verse une solution de glucose et un peu de réactif
de Fehling.
o Le premier tube est laissé à température
ambiante.
o Le second tube est chauffé au bec bunsen.
Questions et interprétation
:
1. La couleur du précipité
obtenu après chauffage est …………………………..
2. La transformation est …………………………?
3. Quelle est l'influence de la température sur cette
transformation ?
Remarque : La liqueur de Fehling
contient des ions Cu2+(aq) complexé par des
ions tartrate en milieu basique.
Le précipité obtenu a pour formule Cu2O(s).
Voir livre page 31.
  Imprimer Imprimer
TP n° 5 : Comment
suivre la cinétique d'une transformation chimique par
titrage ?
Objectif : Etudier l'évolution de la vitesse
volumique de la réaction de l'ion peroxodisulfate avec
l'ion iodure.
Principe : Le diiode formé lentement au
cours de la transformation chimique est dosé par une solution
de peroxodisulfate de sodium.
Les transformations chimiques
mises en jeu :
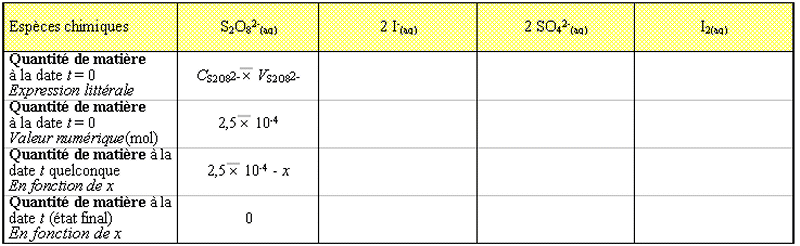
· Réaction lente
entre l'ion peroxodisulfate avec l'ion iodure:
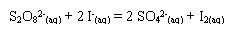
· Réaction rapide
de dosage du diiode par le peroxodisulfate de sodium :
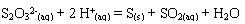
Expérience de suivi
de la cinétique :
· Préparation
de la burette :
o Rincer une première
fois la burette à l'eau.
o Rincer une seconde fois la burette avec la solution de thiosulfate
de sodium. CNa2S2O3 = 1,0 x 10-3 mol.L-1
o Remplir la burette avec la solution de thiosulfate de sodium.
o Ajuster le zéro.
o Veiller à ce qu'il n'y ait pas de bulle d'air sous le
robinet.
· Réaction lente
de l'ion peroxodisulfate avec l'ion iodure :
o Mettre dans un bécher,
50 mL de la solution aqueuse d'iodure de potassium. CKI = 2,5
x 10-1 mol.L-1
o Placer le bécher sur un agitateur magnétique
et mettre en route l'agitation.
o Déclencher le chronomètre au moment où
vous versez 50 mL de la solution aqueuse de peroxodisulfate de
sodium.
CNa2S2O8 = 5,0 x 10-3 mol.L-1
· Prélèvement
et dosage du mélange réactionnel à différentes
dates :
o Prélever 5,0 mL du
mélange avec une pipette jaugée.
o Verser ce volume dans un bécher contenant environ 25
mL d'eau glacée. Ce moment correspond à la date
t à relever au chronomètre.
o Doser le contenu du bécher avec la solution aqueuse
de thiosulfate de sodium de concentration connue.
o Quand la solution est presque incolore (jaune très claire),
ajouter quelques gouttes d'empois d'amidon. Une couleur bleue
apparaît.
o Noter le volume de thiosulfate versé afin d'observer
une disparition de la couleur bleue.
Rôle de l'empois d'amidon
ajouté en fin de réaction
L'empois d'amidon en présence
de diiode est bleu.
A la fin du dosage, c'est à dire lorsque tout le diiode
a réagi avec l'ion thiosulfate, cette couleur bleu disparaît.
L'empois d'amidon est un indicateur de fin de réaction.
o Effectuer cette manipulation
toutes les 5 minutes et noter à chaque fois le volume
de thiosulfate de sodium.
Résultats :
o Compléter le tableau
suivant :
Exploitation des résultats
:
o Tracer le graphe ndiiode
= f(t) en utilisant le tableur excel.
o Imprimer le graphe.
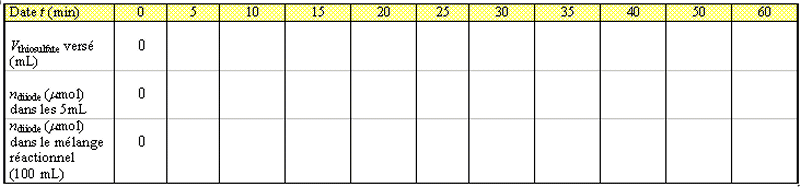
o Faire le bilan de matière
à une date t, pour la transformation chimique mise
en jeu lors de la réaction lente, en faisant intervenir
x, l'avancement de la réaction. Compléter
le tableau ci-dessous.
Réaction lente entre
l'ion peroxodisulfate avec l'ion iodure
Questions :
1. Définir la vitesse
de réaction de formation du diiode.
2. Déterminer graphiquement les vitesses volumiques de
réaction aux dates t0 = 0 min, t1 = 10
min, t2 = 30 min, et t3
= 50 min.
3. Comment évolue la vitesse volumiques de réaction
au cours du temps ? Interpréter.
4. Déterminer graphiquement le temps de demi-réaction
t1/2.
5. Pourquoi verse-t-on chaque prélèvement dans
de l'eau glacée ?
  Imprimer Imprimer
TP n° 6 : Comment
suivre la cinétique d'une transformation chimique par
spectrophotométrie ?
Transformation lente étudiée
: Réduction de l'eau oxygénée par les ions
iodures.
Equation de la réduction
: 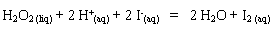
Les quatre étapes du
TP :
1. Détermination de
la longueur d'onde l max correspondant au maximum d'absorption
du diiode.
2. Etablissement de la courbe d'étalonnage C = f(A)
3. Etude de la cinétique par spectrophotométrie.
a. Tracé de la courbe A = f(t)
b. Tracé de la courbe C = f(t)
I. Détermination
de la longueur d'onde l max correspondant au maximum d'absorption
du diiode.
Question préalable :
Pourquoi déterminer lmax ?
Pour obtenir le spectre d'absorption
du diiode, vous disposez de :
- un spectrophotomètre
relié à un ordinateur.
- un logiciel d'acquisition.
|
Les différentes manipulations
informatiques
- Lancer le logiciel SYNCHRONIE
/ Exécuter SYNCHROCHIM / Acquisition / OK
- Choisir SPECTROPHOTOMETRE JENWAY 6300 / COM 1
(le logiciel effectue automatiquement un test)
- Plage de mesure (dans un onglet en dessous)/ Tracé d'un
spectre /
- Début du spectre : 400 nm / Fin du spectre : 600 nm
/ Intervalle de mesure : 5 nm
- Acquisition / Désactiver la mesure de la transmittance
- Cliquer sur Acquisition / Démarrer
- Cliquer sur oui pour recalculer
la ligne de base (faire un blanc)
- Placer la cuve contenant de l'eau distillée.
- Cliquer sur démarrer. |
Attention au sens de la cuve.
La tenir sur les faces striées et la placer tel que les
faces lisses soient dans l'axe du faisceau.
- Introduire la cuve contenant
une solution de diiode de concentration 5 x 10-3 mol.L-1
- Lancer l'acquisition en cliquant sur OK. (Durée environ
5 min).
- Fermer à la fin de l'opération.
On obtient la courbe A = f(l).
Imprimer cette courbe.
Enregistrer sous bureau / spectrophotométrie / courbe
absorbance1
- Déterminer la longueur
d'onde correspondante au maximum d'absorption du diiode.
II. Etablissement de la courbe d'étalonnage C =
f(A)
Question préalable :
Pourquoi établir la courbe d'étalonnage C =
f(A) ?
- Sur le spectrophotomètre.
o Choisir la longueur d'onde
maximale trouvée précédemment.
o Introduire la cuve d'eau distillée et faire un blanc
en appuyant sur CAL
o Introduire la cuve contenant la solution de diiode de concentration
C = 0,5 x 10-3 mol.L-1
o Lire la valeur de l'absorbance.
- Sur le tableur Excel.
o Noter cette valeur et celle
de la concentration sur le tableur Excel.
o Répéter ces opérations (sauf le blanc)
pour les concentrations :
§ C = 1,0 x 10-3
mol.L-1
§ C = 2,0 x 10-3 mol.L-1
§ C = 3,0 x 10-3 mol.L-1
o Tracer le graphe C = f(A)
o Imprimer la courbe.
- Déterminer le coefficient
directeur de la droite obtenue.
III. Etude de la cinétique
par spectrophotométrie.
Question préalable :
quelles grandeurs varient au cours du temps ?
1. Tracé
de la courbe A = f(t)
On effectue deux fois le mélange
suivant dans deux béchers différents notés
bécher reférence et bécher solution :
- 5,0 mL d'acide sulfurique
de concentration 0,5 mol.L-1
- 5,0 mL d'iodure de potassium de concentration 2,0 x 10-1
mol.L-1
- 24,0 mL d'eau distillée.
Remplir la cuve du mélange
du bécher référence. Cette cuve servira
à faire le blanc.
|
Les différentes manipulations
informatiques
- Lancer le logiciel SYNCHRONIE
/ Exécuter SYNCHROCHIM / Acquisition / OK
- Choisir SPECTROPHOTOMETRE JENWAY 6300 / COM 1 (le logiciel
effectue automatiquement un test)
- Plage de mesure
- Longueur d'onde : 490 nm / Temps total : 3 600 s / Intervalle
de temps : 15 s
Attention sur notre spectrophotomètre : le temps affiché
n'est pas le temps réel ; 3600s correspond à 10
min réelles !
- Acquisition / Désactiver la mesure de la transmittance
- Cliquer sur Acquisition / Démarrer
- Cliquer sur oui pour recalculer la ligne de base (faire un
blanc)
- Placer la cuve contenant le contenu du bécher référence.
- Cliquer sur démarrer. |
Début de la cinétique
Une fois que le blanc a été
fait, verser :
- 1,0 mL d'eau oxygénée
de concentration 1,8 x 10 mol.L-1 (solution à
2 volumes)
dans le deuxième bécher.
- Mélanger, remplir
la cuve, et la mettre dans le spectrophotomètre.
- Lancer l'acquisition, en cliquant sur OK.
Attention : cette étape
doit-être réalisée en moins de 15 secondes.
Lorsque l'acquisition est terminée,
cliquer sur fermer.
2. Tracé
de la courbe C = f(t).
- Quitter synchrochim et la
courbe Absor = f(temps) apparaît.
- Sauvegarder le fichier dans bureau / spectrophotométrie
/ courbe absorbance2
- Imprimer le courbe.
- Afin d'obtenir le graphe
C = f(t), remplacer l'ordonnée (Absorbance)
par les concentrations correspondantes en utilisant le résultat
de la courbe d'étalonnage.
- La vitesse volumique de la transformation chimique, en début
de réaction :
o augmente-t-elle ?
o est-elle constante ?
o diminue-t-elle ?
- Déterminer cette vitesse à la date t0
= 0 s.
|