|
  Imprimer Imprimer
TP n° 17 : Qu'est-ce
qui détermine le fonctionnement d'une pile ?
Objectifs :
- Réaliser des piles
avec le matériel mis à ma disposition.
- Compléter les schémas des piles réalisées.
- Mesurer la force électromotrice de la pile.
- Indiquer le sens de circulation du courant électrique.
- Déterminer la polarité de chaque électrode.
- Donner la représentation formelle des piles réalisées.
- Ecrire les équations aux électrodes.
- Ecrire l'équation globale de fonctionnement de la pile.
Matériels :
- Lame de cuivre.
- Lame de fer
- Lame de plomb
- Fil d'argent
- Lame de zinc
- Solution de sulfate de cuivre
CuSO4
- Solution de sulfate de fer II FeSO4
- Solution de nitrate de plomb PbNO3
- Solution de nitrate d'argent AgNO3
- Solution de sulfate de zinc ZnSO4
- Béchers
- Pont salin KNO3
- Voltmètre
Questions :
1. Quel est le métal
le plus réducteur ?
2. Classer du plus réducteur au plus oxydant les différents
couples redox.
3. Quelle pile permet d'obtenir la f.é.m la plus élevée
?
4. Le fonctionnement de la pile dépend-il des couples
mis en jeu ?
5. Proposer un protocole expérimental permettant de montrer
que le fonctionnement de la pile dépend des quantités
de matière présentes.
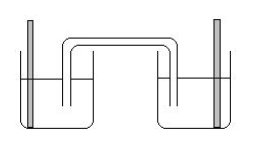 |
 |
|
Représentation
formelle de la pile
............................................................... |
Représentation
formelle de la pile
............................................................... |
|
Equation à cette
électrode //
Equation à cette
électrode
.................................
// ...................................
Equation globale
...................................................... |
Equation à cette
électrode //
Equation à cette
électrode
.................................
// ...................................
Equation globale
.................................................. |
  Imprimer Imprimer
TP n° 18 : Comment
fonctionne un accumulateur ?
On reprend l'une des piles
étudiées lors du TP précédent constituée
des demi-piles Ag+ / Ag et Cu2+ / Cu.
On veut mettre en évidence
comment " recharger " cette pile.
Dans un premier temps, on cherche
à obtenir une pile usée.
Dans un second temps, on souhaite " recharger " cette
pile usée.
I. Obtention de la pile
usée.
1. Constituer la pile 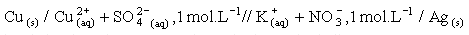
en versant 20 mL de solution dans chaque compartiment de chaque
demi-pile.

Question discussion : Cette
pile est-elle hors équilibre ?
Pour répondre à
cette question,
- Rappeler à partir
des résultats expérimentaux du TP précédent
quel était le sens d'évolution spontanée
de la pile constituée des demi-piles Ag+ /
Ag et Cu2+ / Cu dont l'équation globale est
indiquée sur la feuille réponse.
- Calculer le quotient de réaction dans les conditions
initiales Qr,i = 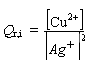 et
comparer sa valeur à celle de la constante d'équilibre
K = 2,15 x 1015. et
comparer sa valeur à celle de la constante d'équilibre
K = 2,15 x 1015.
- Le système est-il hors équilibre ?
2. Brancher entre les deux
électrodes un fil électrique (court-circuit) et
un ampèremètre en série.
Débrancher le fil quand l'intensité est négligeable
(I < 0,01 mA).
Mesurer la tension E aux bornes de la pile à l'aide d'un
voltmètre.
Noter cette valeur dans le tableau de la feuille réponse
(partie II).

Question discussion : Comment
va évoluer le système lors de ce branchement en
court-circuit ?
Répondre sur la feuille réponse.
3. Prélever 1,0 mL à
l'aide d'une pipette graduée de solution dans le compartiment
de l'argent et verser le dans un tube à essai.
Ajouter 2,0 mL de solution de chlorure de sodium saturée.
Observer et conserver le tube comme témoin.

Question discussion : Quel
est l'état du système quand le courant ne passe
plus ?
- A partir de l'observation
précédente, indiquer s'il y a des ions Ag+ dans
le compartiment de l'argent quand le courant ne passe plus ?
Conclusion : Dans ces conditions,
la pile est-elle usée ?
II. Recharge de la pile.
1. Changement du sens d'évolution
spontané du système.
Réaliser le montage
suivant après avoir répondu à la question
:

Question discussion : Comment
doit-on orienter le générateur afin que le sens
du courant imposé permette la recharge de la pile ? (Placer
sur le schéma ci-dessous, la borne positive du générateur).
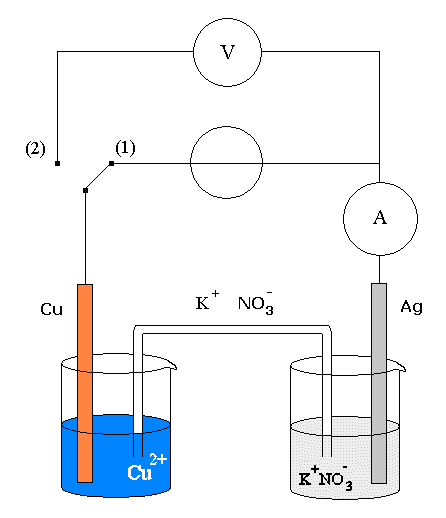
2. Evolution du système
lors de la recharge de la pile.
- Mettre l'interrupteur en
position (1).
- Régler le générateur de façon à
avoir une intensité de l'ordre de quelques milliampères.
- Laisser le courant circuler pendant une quinzaine de minutes
en vérifiant que l'intensité ne varie pas.
- Mesurer la tension aux bornes de la pile au bout de 5 min,
10 min et 15 min en plaçant momentanément l'interrupteur
en position (2). Noter vos résultats sur la feuille annexe.
- Au bout de 15 min, prélever 1,0 mL de solution dans
le compartiment de l'argent et verser le dans un tube à
essai. Ajouter 2,0 mL de solution de chlorure de sodium saturée.

Question discussion :
- Pendant la charge, indiquer
sur le schéma le sens du courant et des électrons.
- En déduire les réactions aux électrodes
et comparer ces réactions à celles quand la pile
débite dans le sens d'évolution spontanée.
Répondre sur la feuille annexe.
- Observer le résultat obtenu lors du test avec la solution
saturée de chlorure de sodium et comparer avec le tube
témoin. Ce test confirme-t-il les réactions aux
électrodes lors de la recharge ?
- En admettant que pendant la charge l'intensité est constante
et égale à I = 5,0 mA, calculer la quantité
d'ions argent formé au bout de 15 min.
Donnée : 1 F : 96500 C.
- En vous aidant du tableau d'évolution du système
à compléter sur la feuille réponse, déterminer
quelle était la quantité d'ions Ag+ présente
dans le bécher quand le système était à
l'équilibre ?
Rappel : K = 2,15 x 1015et V = 20 mL.
- Compléter la conclusion sur la feuille réponse.
  Imprimer Imprimer
Comment fonctionne
un accumulateur ?
Feuille réponse
I. Obtention de la pile
usée.
1. Constitution de la pile
.
- sens d'évolution spontanée
:
……..
2 Ag(+) (aq) + Cu(s) = 2 Ag(s)
+ Cu2+ (aq)
- Quotient de réaction
dans les conditions initiales Qr,i = ……………….
- Comparaison de Qr,i
et de K Qr,i ……… K
- Le système est ……….
équilibre.
2. Branchement en court-circuit.
Sens d'évolution lors du court-circuit :
……..
2 Ag(+) (aq) + Cu(s) = 2 Ag(s)
+ Cu2+ (aq)
3. Etat du système.
- Le résultat du test
avec la solution saturée de chlorure de sodium, nous indique
….………………………
Conclusion : …………………………………………………………………………………………………..
II. Recharge de la pile.
1. Changement du sens d'évolution
spontanée du système.
2. Evolution du système lors de la recharge de la pile.
- Lorsque la pile est en recharge
:
Réaction à l'électrode
de cuivre : …………………………………
Réaction à l'électrode d'argent : …………………………………
- Lorsque la pile débite
(sens d'évolution spontanée) :
Réaction à l'électrode
de cuivre : …………………………………
Réaction à l'électrode d'argent : …………………………………
- Evolution de la tension :
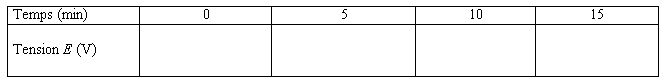
- Le test avec la solution
saturée de chlorure de sodium nous indique.............................................................
- Quantité d'ions formés
(mol) : ……………………………………………………………………….
- Tableau d'évolution
du système :
|
|
2 Ag+(aq) |
Cu(s) |
2 Ag(s) |
Cu2+(aq) |
|
Etat initial (mol) |
0 |
beaucoup |
beaucoup |
0,020 |
|
Etat intermédiaire(mol) |
|
beaucoup |
beaucoup |
|
Etat final (mol)
(quand I négligeable) |
|
beaucoup |
beaucoup |
|
- Détermination de xfinal
quand le système est à l'équilibre :
- Conclusion : on peut, dans
certains cas, changer le sens …………………………….
d'un système en imposant un courant de sens …………………..
à celui observé lorsque le système évolue
spontanément. On dit que la transformation est ………………………..
|